Члени робочої групи з підготовки рекомендацій: акад. НАМН України, проф. В.М. Коваленко, проф. Сичов О.С., проф. М.М. Долженко, проф. Ю.А. Іванів, к.м.н. С.І. Деяк, к.м.н. С.В. Поташев
Клапанна регургітація є однією з важливих причин серцево-судинної захворюваності та смертності. Ехокардіографія (ЕхоКГ) сьогодні є головним неінвазивним методом візуалізації при оцінці клапанної регургітації (КР). Ехокардіографічна оцінка КР повинна поєднувати якісне та кількісне її визначення, оцінку анатомії та функції клапану, так само, як і наслідки клапанної патології та її вплив на анатомію та функцію камер серця. В клінічній практиці ведення пацієнтів в великій мірі залежить від результатів ехокардіографічного обстеження. Тому забезпечення стандартів з метою визначення базового переліку обов’язкових вимірів при оцінці клапанної регургітації є критичним.
Ключові слова: клапанна регургітація, ехокардіографія, рекомендації, мітральний клапан, трикуспідальний клапан
Вступ
Допплерівська ехокардіографія (ЕхоКГ) є незамінною методикою при початковій діагностиці та динамічному спостереженні у пацієнтів з клапанною недостатністю. Вона надає детальну інформацію про анатомію та функцію клапана та дозволяє визначити механізми клапанної регургітації (КР). Допплерівська ЕхоКГ (ДЕхоКГ) не тільки виявляє факт наявності регургітації, але й дозволяє зрозуміти її механізм, кількісно визначити важкість її наслідків [1-3]. В клінічній практиці тактика ведення пацієнтів в великій мірі залежить від результатів ехокардіографічного обстеження. Тому забезпечення стандартів з метою визначення базового переліку обов’язкових вимірів при оцінці клапанної регургітації є критичним.
На практиці оцінка клапанної регургітації вимагає використання різних ехокардіографічних модальностей з поєднанням множинних параметрів, що потребують співставлення з об’єктивними клінічними даними. Метою даного документа є сумація наявних сьогодні стандартів з оцінки нативної клапанної недостатності атріо-вентрикулярних (АВ-) клапанів [2,3].
Загальні рекомендації
Двохвимірна (2D) трансторакальна ЕхоКГ (ТТЕ) є рекомендованою у якості методу візуалізації «першої лінії» при КР, та часто є достатньою для встановлення коректного діагнозу. Двохвимірна черезстравохідна ЕхоКГ (ЧСЕ) показана, коли проведення ТТЕ є недостатнім для чіткого кількісного діагнозу чи потрібно підвищення рівня діагностики. Трьохвимірна (3D) ЕхоКГ забезпечує реалістичні та інтуїтивні анатомічні зображення клапанного апарату, що може надати додаткову інформацію, особливо у пацієнтів із складними клапанними ураженнями, та дозволяє забезпечити більш чітке кількісне визначення гемодинамічних наслідків КР на порожнини серця [4].
|
Оцінка клапанів: рекомендації
1. ТТЕ рекомендована як візуалізаційна методика «першої лінії» при клапанній регургітації.
2. ЧСЕ є показаною, колі дані ТТЕ не є діагностичними або для підвищення якості діагнозу.
3. Трьохвимірна ЕхоКГ може забезпечити додаткову інформацію у пацієнтів із складними клапанними ураженнями.
4. ЧСЕ не є показаною у пацієнтів з доброю якістю ТТЕ окрім випадків в операційній підчас виконання хірургічного втручання на клапані.
|
На практиці оцінка клапанної регургітації починається з 2D-ТТЕ, яка в більшості випадків дозволяє диференціювати ступінь важкості регургітації від незначущою фізіологічної при нормальній клапанній анатомії та рухливості стулок до важкої при наявності значного клапанного дефекту. Етіологія та механізм регургітації (ураження/деформація, що призводить до клапанної дисфункції) включаючи тип дисфункції (аномальний рух стулок) описуються відповідно до класифікації рухомості стулок за Карпент’є:
· Тип I: нормальний рух стулок;
· Тип ІІ: надлишковий рух;
· Тип ІІІ: обмеженний рух (рестрикція) стулок [5].
Далі, ретельна оцінка регургітуючого потоку підчас кольорового допплерівського картування (КДК) з використанням множинних зрізів може віддиференціювати мінімальну регургітацію, що не потребує подальшої оцінки від більш важких випадків, коли рекомендована більш кількісні методики оцінки (vena contracta (VC); проксимальна площа ізошвидкісної поверхні (PISA)).
|
Оцінка важкості клапанної регургітації: рекомендації
1. Площа регургітуючого потоку в КДК не рекомендується для оцінки ступеня важкості клапанної регургітації.
2. Як визначення VC, так і PISA рекомендуються для оцінки ступеня важкості регургітації, де можливо їх визначення.
3. При неспівпадінні між даними різних методів кількісної оцінки важкості регургітації та об’єктивними клінічними даними слід використовувати додаткові параметри.
|
Другим кроком є оцінка впливу регургітації на шлуночки, передсердя та визначення тисків переднавантаження (тиск в лівому передсерді, тиск в малому колі кровообігу, центральний венозний тиск). Розміри та функція шлуночків визначаються використанням розмірів та/чи об’ємів (біплановий метод дисків за Симпсоном в 2D або визначення об’ємів в 3D-Ехокг при адекватній якості зображення) (Рис. 1). Слід пам’ятати, що фракція викиду (ФВ) залежить від навантаження та часто переоцінює реальну систолічну функцію шлуночка. Сьогодні доступні нові параметри оцінки функції шлуночків (швидкість руху міокарду, деформація міокарду за даними 2D-стрейну, або strain rate) для кращої оцінки міокардіальної функції шлуночків, але вони ще потребують валідації та обґрунтування більшими серіями пацієнтів з КР. Об’єми передсердь можуть надійно визначатися біплановими методами дисків або по формулі «площа-довжина» чи за допомогою 3D-ЕхоКГ. Методика отримання результатів, переваги та обмеження різних допплерівських параметрів оцінки важкості регургітації деталізовані в Таб. 1 та 2.
Наприкінці отримані дані мають співставлятися з індивідуальними клінічними об’єктивними даними з метою стратифікації тактики ведення хворого та його динамічного спостереження [6]. При показаннях у випадках регургітації на клапанах лівих відділів кількісна стрес-ЕхоКГ може допомогти в диференційній діагностиці важкої регургітації, що в спокої може бути недооціненою, як помірна, а також наслідки цієї регургітації для лівих відділів та малого кола кровообігу. Використання стрес-ЕхоКГ при клапанній хворобі серця має бути викладена в іншому документі [7]. Рішення про динамічне спостереження та лікувальну тактику має бути прийнятим відповідно до клінічного об’єктивного статусу пацієнта та ступеня важкості регургітації [6].
|
Розмір та функція ЛШ: рекомендації
1. Кількісна оцінка розмірів, об’ємів та фракції викиду (ФВ) лівого шлуночка (ЛШ) є обов’язковою.
2. Слід віддавати перевагу визначенню поперечних розмірів ЛШ у 2D, особливо якщо неможливо встановити курсор М-режиму перпендикулярно довгій вісі ЛШ.
3. Для визначення об’ємів та ФВ ЛШ в 2D рекомендується використовувати метод біпланової сумації дисків за Симпсоном.
4. Оцінка функції ЛШ у 3D забезпечує більш точні та відтворювані дані.
5. У пацієнтів з поганим акустичним вікном показане проведення ЕхоКГ з контрастуванням.
6. Якісна оцінка функції ЛШ не є рекомендованою.
7. Для оцінки розмірів лівого передсердя (ЛП) рекомендованим є визначення його об’єму.
|
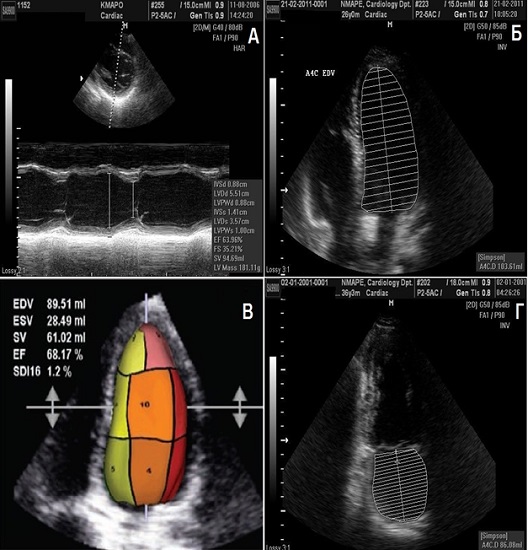
Рис. 1. (А) Визначення розмірів ЛШ в M-режимі; (Б) оцінка об’ємів та ФВ ЛШ сумаційним методом дисків за Симпсоном; (С) оцінка об’ємів ЛШ в 3D; (Г) оцінкаобєму ЛП сумаційним методом дисків.
Таб. 1. Ехокардіографічні параметри, що використовуються для кількісної оцінки важкості недостатності клапанів магістральних артерій: записи.
|
Параметри
|
Аортальна регургітація (АР)
|
Регургітація на КЛА (ЛР)
|
|
Морфологія клапану
|
Візуальна оцінка
Множинні позиції
|
Візуальна оцінка
Множинні позиції
|
|
Регургітуючий потік в КДК
|
Оптимізація підсилення / шкали картування
Парастернальні позиції по довгій та короткій осі
|
Оптимізація підсилення / шкали картування
Парастернальна позиція по короткій осі
|
|
Ширина VC
|
Перевага віддається PLAX (А4С як альтернатива)
Оптимізація підсилення / шкали картування
Ідентифікація трьох компонентів регургітуючого потоку
(VC, PISA, потік в ЛШ)
Зменшення розміру сектора КДК та глибини сканування для максимізації частоти зміни кадрів
Збільшення цієї зони (режим «zoom»)
Пошук кращого кадру трекболом для вимірів
Вимір найменшої VC
(безпосередньо за регургітуючих отвором перпендикулярно напрямку потока)
|
Парастернальна позиція по короткій осі
Оптимізація підсилення / шкали картування
Ідентифікація трьох компонентів Зменшення розміру сектора КДК та глибини сканування для максимізації частоти зміни кадрів
Збільшення цієї зони (режим «zoom»)
Пошук кращого кадру трекболом для вимірів
Вимір найменшої VC
|
|
Метод PISA
|
А5С позиція для центральних потоків / PLAX для ексцентричних
Оптимізація кольорового спектру потоку АР
Зображення в режимі «zoom»
Підвищення ліміту Найквіста в апікальних позиціях / зниження або підвищення в PLAX
Обрати найкращу PISA трекболом
Визначити радіус PISA по лінії напрямку курсора
Визначити пікову швидкість та VTI потоку АР (CW) –
Розрахунок швидкості, ПЕРО та ОР
|
Парастернальна позиція по короткій осі
Оптимізація кольорового спектру потоку ЛР та збільшити зони зацікавленості («zoom»)
Зменшення ліміту Найквіста (нульова лінія кольорового спектру)
Визначити радіус PISA в середині систоли
по лінії напрямку курсора
Визначити пікову швидкість та VTI потоку ЛР (CW) –
Розрахунок швидкості, ПЕРО та ОР
|
|
Спектр регургітації в CW
|
А5С
|
Парастернальна позиція по короткій осі
|
|
Час напів-зниження тиску (РНТ)
|
А5С
CW
|
Парастернальна позиція по короткій осі в CW
|
|
Реверсія діастолічного потоку в нисхідній аорті
|
PW Doppler
Проксимальна нисхідна Ао / Брюшна Ао
|
-
|
|
Розмір шлуночка
|
Перевага віддається оцінці об’ємів ЛШ за Симпсоном
|
Перевага віддається вимірам розмірів ПШ в А4С позиції
|
Таб. 2. Ехокардіографічні параметри, що використовуються для кількісної оцінки важкості клапанної регургітації: переваги та обмеження.
|
Параметри
|
Корисність/переваги
|
Обмеження
|
|
Морфологія клапану
|
Патологічна рухомість клапану є специфічною для важкої регургітації (напр. відрив хорди чи папілярного м’яза при МР)
|
Інші морфологічні аномалії не є специфічними для важкої клапанної регургітації
|
|
Діаметр трикуспідального кільця при ТР
|
Дилатація – чутлива ознака важкої ТР
|
Дилатація трапляється і при інших патологічних станах
Потребує доказового підтвердження в клінічних випробуваннях
|
|
Потік регургітації в КДК
|
Простота використання
Дозволяє оцінити просторову орієнтацію регургітуючого потоку
Добрий скрінінговий тест для диференціації легкої vs. важкої регургітації
|
Може бути неточним для оцінки важкості регургітації
На оцінку впливають технічні та гемодинамічні фактори
Розповсюдження за межі регургітуючого отвору при АР чи ЛР є непередбачуваним, і тому не може бути використане для оцінки важкості
Ексцентричний потік, що тече по стінці передсердя, може призводити до недооцінки важкості МР чи ТР (ефект Коанда)
|
|
Ширина VC
|
Відносно швидкий та легкий у використанні
Відносно незалежний від гемодинамічних та інструментальних факторів
Недостатність інших клапанів не впливає на відтворюваність
Добре диференціювати легку vs. важку регургітацію
Може використовуватися при ексцентричних регургітуючих токах
|
Не підходить за наявності декількох струменів потоку регургітації
При маленьких значеннях помилки у вимірюванні призводять до великого % похибки
Проміжні значення потребують відтворюванного підтвердження
На значення впливають систолічні зміни регургітуючого потоку
Замало літературних даних щодо VC при ЛР
|
|
Метод PISA
|
Може використовуватися при ексцентричних регургітуючих токах
Етіологія регургітації чи недостатність іншого клапану не впливають на відтворюваність
Кількісна оцінка: оцінює важкість ураження клапану (ПЕРО) та об'ємне навантаження (Об'єм регургітації)
Конвергенція потоку при ліміті Найквіста >50 см/с вказує на значущу МР
Велика конвергенція потоку при ліміті Найквіста 28 см/с вказує на значущу ТР
|
На контур PISA впливає швидкість еліейзингу (ліміту Найквіста) у випадку не циркулярного регургітуючого отвору при систолічних змінах контурів прилеглих до отвору структур
Радіус PISA більше нагадує напівеліпс
Помилка при вимірі PISA возводиться в квадрат
Досить велика варіабельність у різних виконавців
Не може використовуватися при декількох струменях регургітації
Вимірювання утруднене при АР з кальцифікацією клапанних структур
При ТР валідовано невеликою кількістю досліджень
Замало літературних даних при ЛР
|
|
Спектр регургітуючого потоку в CW
|
Простота, легкість відтворювання
|
Якісна допоміжна характеристика
Важко отримати повний спектр при ексцентричному струмені регургітації
|
|
Час напівзниження тиску (РНТ) при АР чи ЛР
|
Простота
|
На параметр впливають комплаєнс ЛШ, артеріальний тиск, гострота виникнення патологічного потоку
|
|
Реверсія діастолічного потоку в нисхідній аорті при АР
|
Простота
|
На параметр впливають позиція пробного об’єму та гострота виникнення АР
На параметр впливає комплаєнс аорти
Короткочасна ранньо-діастолічна реверсія потоку є варіантом норми
|
|
Кровопотік в легеневих венах при МР
|
Простота
Реверсія систолічного потоку специфічна для важкої МР
|
На параметри впливають тиск в ЛП, фібриляція передсердь
Не є показовим, якщо струмінь МР спрямований в легеневу вену, в якій оцінюється потік
|
|
Кровопотік в печінкових венах при ТР
|
Простота
Реверсія систолічного потоку специфічна для важкої ТР
|
На параметри впливають тиск в ПП, фібриляція передсердь
|
|
Швидкість піку E при МР чи ТР
|
Простота, легкість відтворювання Звичайно підвищується при важкій регургітації
|
На параметр впливають тиск в передсерді, фібриляція передсердь, діастолічна функція шлуночка
Допоміжний параметр
|
|
Розмір передсердь та шлуночків
|
Дилатація – чутлива ознака хронічної важкої регургітації
Нормальні порожнини майже повністю виключають важку регургітацію
|
Дилатація спостерігається при інших патологічних станах (неспецифічні параметри)
Можуть бути нормальними при важкій регургітації, що виникла гостро
|
Аортальна регургітація
Аортальна регургітація (АР) є розповсюдженою клапанною патологією. ЕхоКГ відіграє цінну роль в оцінці та лікуванні хворих з АР [1-3].
Анатомія та функція аортального клапану
Аортальний клапан (АК) складається з комплексу структур, оточуючих аортальний отвір (АО) увздовж виносного тракту ЛШ (ВТЛШ) [8]. Типово, АК має три напівлунних за контуром стулки. Стулки «вставлені» в фіброзний «рукав», прикріплений до медії аорти (Ао) зверху (синуси Вальсальви та сино-тубулярний перехід). Знизу стулки прикріплені до міокарду ВТЛШ та передньої стулки мітрального клапану (МК) (віртуальне базальне кільце) нижче анатомічного шлуночкові-аортального переходу. Таким чином, справжнє анатомічне аортальне кільце – це не проекція на рівні базального прикріплення стулок, як часто визначають в літературі та вимірюється різними візуалізацій ними методиками, а короноподібна трьохвимірна структура. Слід відмітити, що на розмір аортального кільця та кореня впливає внутрішній тиск, що динамічно змінюється протягом серцевого циклу. Кожна стулка прикріплена увздовж свого контуру, зустрічаючись одна з одною у трьох комісур, що знаходяться на рівніх відстанях по колу «рукава» надаортального гребінця. В нормальному АК стулки симетричні, мобільні та вільні у комісур, з рівним ступенем коаптації при закритті. Стулки носять назви лівої та правої коронарної, та не коронарної відповідно до розташування гирл коронарних артерій.
Етіологія та механізми АР
АР є наслідком патології стулок АК або дилатації кореня Ао, що призводить до їх розтягнення та зашкоджує їх нормальній коаптації. Звичайними причинами порушення морфології стулок, що призводить до АР включають дегенеративний віковий кальциноз стулок, 2-стулковий АК, інфекційний ендокардит та ревматичні вади. Причини з боку кореня Ао включають ануло-аортальну ектазію (ідіоматична дилатація кореня), синдром Марфана, розшарування Ао, хвороби патології колагену артерій та сифилис. Для описання механізму АР звичайно використовують класифікацію Карпент’є (Рис. 1, Таб. 3) [9].
Ключові моменти: у пацієнтів з АР необхідний детальний аналіз морфології області АК. Заключення ЕхоКГ має включати інформацію про етіологію, ступінь процесу та тип дисфункції. У випадку «чистої» АР слід також відзначити потенційну можливість оперативного лікування.
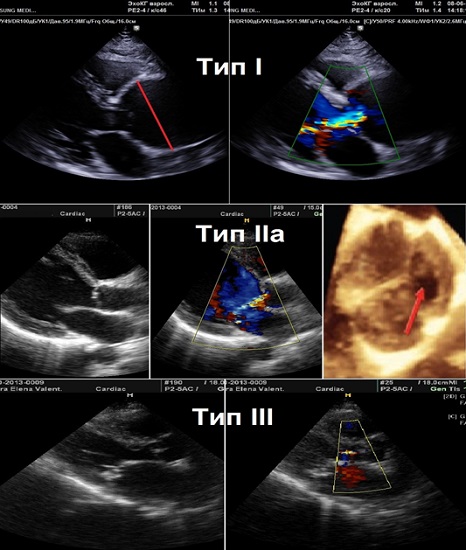
Рис. 1. Механізми АР згідно функціональної класифікації Карпент’є.
Тип І: дилатація аортального кільця. Тип ІІа: пролапс стулки (стрілка). Тип ІІІ: ревматична вада АК з обмеженням руху стулок.
Таб. 3. Функціональна класифікація анатомічних уражень при АР.
|
Дисфункція
|
Ехо-знахідки
|
|
Тип I: збільшення кореня Ао при нормальних стулках
|
Дилатація будь-яких компонентов кореня Ао (аортальне кільце, синусів Вальсальви, синотубулярного переходу)
|
|
Тип IIa: пролапс стулки з ексцентричним потоком АР
|
|
Стулка, що молотить
|
Повне вивертання стулки в діастолу в ВТЛШ в позиціях по довгій осі
|
|
Частковий пролапс стулки
|
Дистальна частина стулки пролабує в ВТЛШ (чітке прогинання тіла стулки в позиціях по довгій осі та наявність маленького циркулярного дефекту структури біля вільного краю стулки по короткій осі)
|
|
Повний пролапс стулки
|
Вільний край стулки перетинає площину аортального кільця з вибуханням всього тіла стулки в ВТЛШ (наявність великого циркулярного чи овального дефекту структури безпосередньо під АК по короткій осі)
|
|
Тип IIb: фенестрація вільного краю стулки з ексцентричним потоком АР
|
Наявність ексцентричної АР без чіткого свідоцтва пролабування стулок
|
|
Тип III: порушення анатомії / кількості стулок
|
Потовщений ригідний клапан з обмеженням руху
Деструкція тканини (ендокардит)
Великі участки кальцинозу / екстенсивний кальциноз всіх стулок, що утруднює рух стулок
|
|
Ступінь кальцинозу АК визначається наступним чином:
Ст. 0 (-): кальцинозу немає
Ст. 1 (+): кальциноз кореня / ізольовані маленькі локуси кальцинозу.
Ст. 2 (++): більші участки кальцинозу / країв стулок.
Ст. 3 (+++): розповсюдження кальцинозу на тіла стулок / певне утруднення руху стулок.
Ст. 4 (++++): тотальний кальциноз стулок з обмеженням їх руху (відповідає стенозу АК).
|
Ехокардіографічна оцінка АР
Класично для виміру ВТЛШ, Ао кільця та синусів Вальсальви використовують парастернальну позицію по довгій осі ЛШ. Товщина та мофологія стулок оцінюється до довгій та короткій осях з парастернального доступу та в апікальних 5- (А5С) та 3-камерних (А3С) позиціях. Втім, часто ТТЕхоКГ в В-режимі не дозволяє здійснити повну оцінку анатомії та причин АР. В цих ситуаціях кращу оцінку морфології дозволяє 3D-ЕхоКГ [4,8]. В деяких випадках ЧСЕхоКГ потрібне саме коли ТТЕхоКГ не дозволяє з’ясувати механізми та причини АР, так само як і отримати виміри та морфологію кореня Ао [9].
Знахідки при АР в В- та М-режимі
Має забезпечуватися інформація про патологію стулок (надмірність, рестрикція, довжина стулок, адекватність коаптації, мобільність/податливість, товщина, цілісність), стан комісур (злиття, вивих, місце прикріплення, вирівнювання) та морфологію кореня Ао (гіпертрофія МШП, розміри кільця, синусів та сино-тубулярного переходу, висхідної Ао). Наявність патологічно рухливої стулки специфічна для важкої АР. Крім того, слід шукати непрямі додаткові ознаки, асоційовані з АР, в В- (діастолічне прогинання передньої стулки МК в діастолу, гіперехогенність базальної МШП) та М-режимі (високочастотне діастолічне тремтіння передньої стулки МК, або хорд МК (симптом «півнячого гребінця»), або МШП, передчасне закриття МК, передчасне пізньо-діастолічне закриття АК) (Рис. 3, 4).
Ключові моменти: додаткові ехо-знахідки використовуються як допоміжні параметри оцінки важкості АР. Оцінка морфології та розмірів області кореня Ао є обов’язковими.
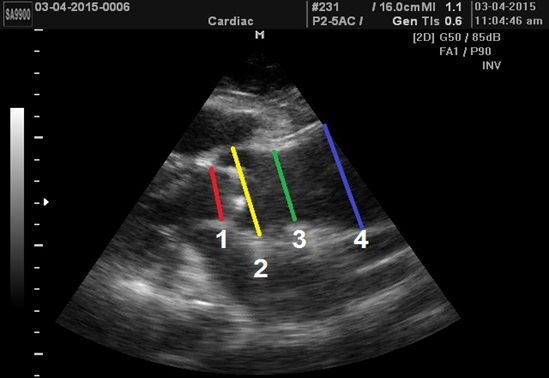
Рис. 3. Виміри розмірів Ао (1 – діаметр ВТЛШ; 2 – діаметр кореня Ао (синусов Вальсальви); 3 – діаметр синотубулярного переходу; 4 – діаметр висхідної Ао).
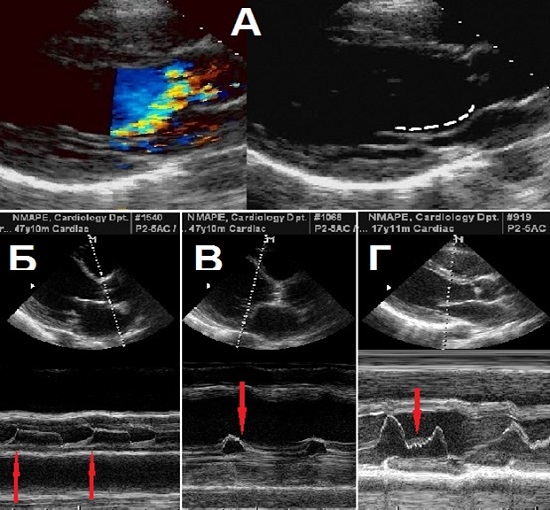
Рис. 4. Додаткові ознаки вираженої АР в В- та М-режимі. А. Діастолічне прогинання передньої стулки МК в діастолу. Б. Передчасне пізньо-діастолічне відкриття АК
Оцінка важкості АР
Кольорова допплерографія
Кольорове допплерівське картування (КДК). Використовуючи КДК в багатьох доступах можна візуалізувати поток регургітації через АК в ЛШ в діастолу. Площа та довжина струменя АР слабо корелюють із ступенем важкості АР, тому що на них впливають діастолічний градієнт тиску між Ао та ЛШ, та податливість ЛШ, а також тому що в апікальних позиціях його дуже легко переоцінити. Сьогодні площа та довжина потоку АР в КДК не є рекомендованими для визначення важкості АР. Практично, КДК служить для виявлення та початкової візуальної оцінки АР. Центральний струмень АР частіше буває при ревматичних вадах та при аневризмах кореня Ао, а ексцентричні потоки АР частіше асоціюються з пролабуванням чи перфорацією стулок АК. Кольорове картування в М-режимі допомагають виявити поведінку потоків в часі (Рис. 5).
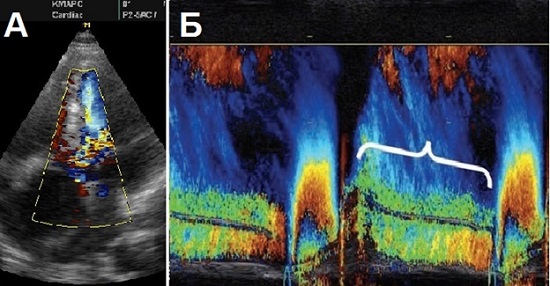
Рис. 5. А. КДК в А5С: важка АР при ідіопатичній аневризмі Ао. Б. КДК в М-режимі відображує поведінку потоку АР в часі.
Діаметр струменя та поперечна площа потоку в самому його початку під регургітуючим отвором є напівкількісними показниками важкості АР в ЦДК. Максимальний діаметр кольорового струменя (ширина) вимірюється в діастолу безпосередньо під АК (на з’єднанні ВТЛШ та Ао кільця) в парастернальній позиції по довгій осі. Ширина струпеня є пропорційною до розміру дефекту АК. Втім, цей принцип має на увазі циркулярний регургітуючих отвій. Тому, якщо контур регургітуючого отвору є неправильним, як, наприклад, при 2-стулковому АК, ширина струменя АР буде менше корелювати зі ступенем регургітації. Тому більш точним є співвідношення ширини струменя до діаметру ВТЛШ. Площа поперечного зрізу АР з парастернальної позиції по короткій осі та її відношення до площі ВТЛШ такоє є напівкількісним показником важкості АР. Хоча ці виміри є схільними до високої варіабельності при виконанні різними дослідниками, співвідношення ширини струменя до діаметру ВТЛШ >65% є сильним аргументом на користь важкої АР [10].
Ключові моменти: не рекомендується для кількісного визначення важкості АР використання ізольованого показника площі регургітуючого потоку АР. КДК слід використовувати тільки для візуальної оцінки АР. При більш, ніж маленькому центральному потоку АР потрібен більш кількісний підхід.
Ширина VC. При АР візуалізація VC, регургітуючого потоку відразу по перетині регургітуючого отвору, здійснюється в парастернальній позиції по довгій осі [11-13]. Практично, VC представляє собою найменший діаметр потоку на рівні АК в ВТЛШ безпосередньо під областю конвергенції потоку (Рис. 6). Таким чином, вона забезпечує оцінку площі ефективного регургітуючого отвору (ПЕРО), та є меншою, ніж ширина регургітуючого потоку далі в ВТЛШ (розповсюдження потоку далі в глибину). При використанні ліміту Найквіста 50–60 см/с ширина VC <3 мм корелює з легкою АР, в той час, як ширина >6 мм вказує на важку АР. На вимір VC впливає декілька факторів, наприклад, наявність декількох струменів. В такій ситуації відповідні діаметри різних VC не сумуються. Концепція VC базується на припущенні, що регургітуючих отвір майже правильно круглий. Фактично ж, отвір має еліптичний чи неправильний контур, коли ширина VC в різних позиціях може бути різною. Було показано, що КДК в 3D-ЕхоКГ може бути корисним при візуалізації істинного контуру регургітуючого отвору [13].
Ключові моменти: Вимір діаметру VC рекомендується для оцінки важкості АР, коли можливо. Проміжні значення VC (3-6 мм) потребує підтвердження більш кількісними значеннями, коли це можливо. VC звичайно можна виміряти навіть при ексцентричних потоках АР. У випадку множинних струменів діаметри відповідних VC не сумується. Оцінка VC в 3D досі потребує доказової бази.
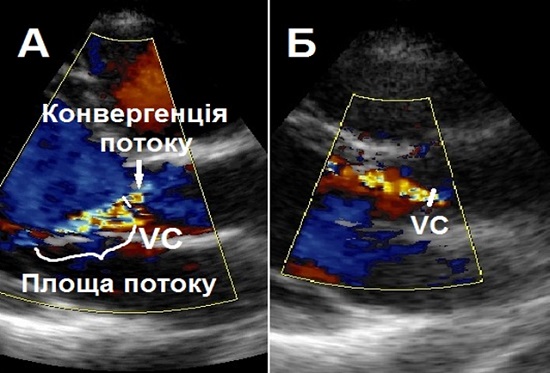
Рис. 6. А. Напівкількісна оцінка важкості АР за допомогою ширини vena contracta (VC). В парастернальній позиції по довгій осі візуалізуються три компонента регургітуючого потоку: зона конвергенції потоку (PISA), VC та турбулентний потік в ВТЛШ. Б. Оцінка VC у пацієнта з потоком АР, направленим в бік МШП.
Метод конвергенції потоку. Оцінка зони конвергенції потоку при АР вивчалася менш детально, ніж при мітральній регургітації (МР) [14,15]. Зона конвергенції потоку візуалізується з А3С або А5С, або з парастернальної позиції по довгій осі, або з верхніх правих парастернальних доступів. Радіус PISA вимірюється в діастолу, використовуючи перший еліейзінг. Об'єм регургітації (ОР) та площу ефективного регургітуючого отвору (ПЕРО) розраховують за стандартними формулами (Рис. 7 та 8). Метод оцінки конвергенції потоку (PISA) має декілька обмежень. По перше, його не можливо застосувати у значного відсотка хворих з АР через перешкоди тканиною клапану та важкості коректної ідентифікації зони конвергенції. Не плоский або обмежений контур зон конвергенції, що спотворюють напівсферичне припущення є потенційними причинами недо- або переоцінки важкості АР цим методом. Відповідно, метод PISA повинен з обережністю застосовуватися у пацієнтів з тупими кутами конвергенції, як при аневризматичному розширені висхідної Ао, чи при обмеженою зоною конвергенції потоку, що може спостерігатися у пацієнтів з перфорація ми стулок чи комісуральними регургітаціями. Класифікація ступеней АР за методом PISA визначає важкість як легку, помірну та важку з підрозділом помірної АР на «легку помірну» (ПЕРО 0,1-0,19 см2, ОР 20–44 мл) та «важку помірну» чи «виражену» (ПЕРО 0,2-0,29 см2, ОР 45-59 мл). ПЕРО ≥0,3 см2 або ОР ≥60 мл вказує на важку АР.
Ключові моменти: коли можливо, метод PISA є високо рекомендованим для кількісної оцінки АР. Він може використовуватися як при центральних, так і ексцентричних потоках. При ексцентричних потоках для оцінки конвергенції потоку рекомендується використовувати парастернальну позицію по довгій осі. ПЕРО ≥0,3 см2 або ОР ≥60 мл вказує на важку АР.
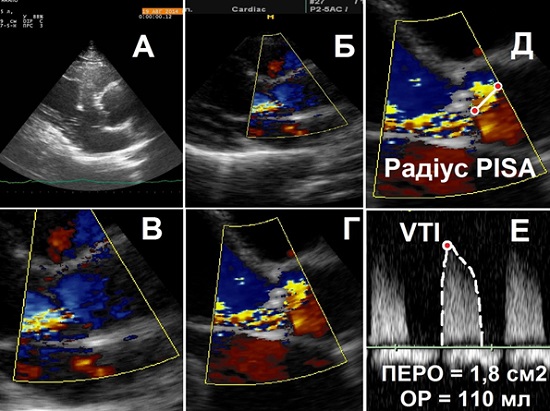
Рис. 7. Кількісна оцінка важкості АР за методом PISA при важкій ревматичній АР. Послідовний аналіз АР: А. Парастернальна позиція по довгій осі ЛШ. Б. КДК потоку АР. В. Режим «zoom» обраної зони. Г. Зсув нульової лінії кольорової шкали для отримання гемісфери PISA. Д. Вимір радіусу PISA до першого накладення спектру (еліейзингу). Е. CW-допплер АР для розрахунку площі ефективного регургітуючого отвору (ПЕРО) та об’єму регургітації (ОР)
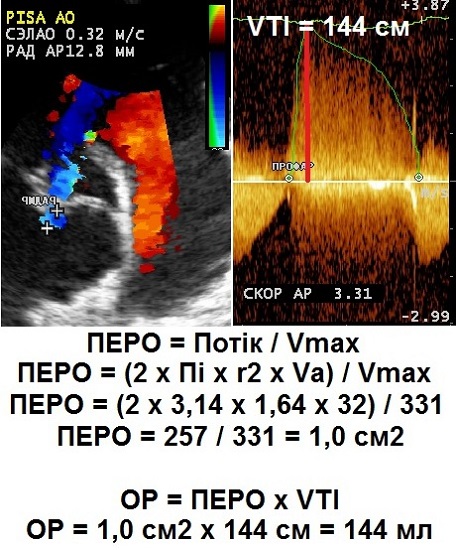
Рис. 8. Кількісна оцінка важкості АР при аневризмі Ао методом PISA з А5С позиції. ПЕРО – ефективний регургітуючий отвір; ОР – об'єм регургітації; VTI – інтеграл лінійної швидкості потоку; Va – швидкість еліейзінгу; Vmax – пікова швидкість регургітації.
Імульсний допплер
Допплерівський волюмометричний метод. Імпульсний допплер (PW) може бути альтернативним методом кількісної оцінки важкості АР [1-3]. За відсутності значної МР мітральний діастолічний потік використовується для розрахунку системного ударного об’єму. Позиція на КЛА може використовуватися у пацієнтів із значною МР. Тотальний ударний об'єм розраховується з розрахункового ударного об’єму в ВТЛШ. Цей метод займає багато часу та асоціюється з декількома недоліками. Але взагалі, фракція регургітації (ОР, поділений на ударний об'єм в ВТЛШ) >50% вказує на важку АР.
Реверсія діастолічного потоку в нисхідній Ао (або в периферичних артеріях). АР може призводити до реверсії діастолічного потоку в Ао. Найкраще це можна візуалізувати в верхній частині нисхідної Ао з супрастернального доступу, використовуючи PW. Пробний об'єм встановлюється трошки дистальніше гирла лівої підключичної артерії з курсором максимально паралельно довгій осі нисхідної Ао. Допплерівський фільтр встановлюється на найнижчі значення для фіксації низьких швидкостей (<10 см/с). При більш легких ступенях АР спостерігається коротка реверсія потоку, обмежена ранньою діастолою. По мірі збільшення ступеня регургітації тривалість та швидкість реверсивного потоку зростають. При важкій АР він триває всю діастолу (голодіастолічний потік) з максимальною швидкісю вище 20 см/с (кінцево-діастолічна швидкість, що співпадає з зубцем R ЕКГ) (Рис. 9). Це порогове значення валідовано для проксимального сегменту нисхідної Ао [16]. Значний голодіастолічний реверсивний потік в абдомінальній Ао також є дуже специфічною ознакою важкої АР.
Ключові моменти: визначення реверсії діастолічного потоку в нисхідній та брючній Ао є рекомендованим у всіх пацієнтів, в яких можна його візуалізувати. Це один з найпотужніших додаткових параметрів оцінки важкості АР.
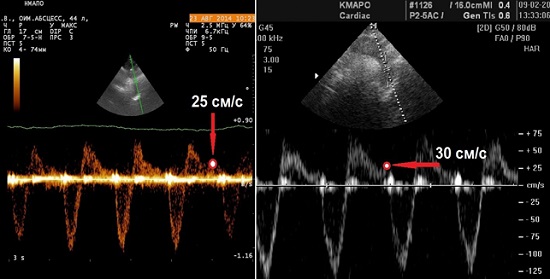
Рис. 9. Запис в PW-допплері в нисхідній Ао у пацієнтів з важкою АР з інфекційним ендокардитом (зліва) та ідіопатичною аневризмою Ао (зправа) демонструє голодіастолічний зворотний потік з кінцево-діастолічними швидкостіми >20 см/с.
Постійний допплер потоку АР
Постійний допплер (CW) класично найкраще отримується з А5С позиції (Рис. 10). Втім, слід використовувати ту позицію, в якій курсор буде максимально паралельним направленню потоку. Іноді при ексцентричних потоках кращий допплерівський сигнал може бути отриманий з правого парастернального вікна. Для легкої АР характерний «блідий» CW-спектр.
Щільний допплерівський спектр може бути характерним як для помірної, так і важкої АР. Тобто практично щільність CW-спектру не дає корисної інформації щодо важкості АР. Швидкість сповільнення діастолічного регургітуючого потоку та розрахунковий час напізниження тиску (РНТ) відбивають як ступінь АР, так і кінцево-діастолічний тиск в ЛШ. По мірі зростання важкості АР знижується діастолічний тиск в Ао та зростає кінцево-діастолічний тиск в ЛШ [17,18]. Таким чином зменшується кінцево-діастолічна швидкість потоку регургітації із скороченням РНТ. РНТ<200 мс визначає важку АР. РНТ >500 см говорить про легку АР. Слід відмітити, що на значення РНТ впливає еластичність та податливість (комаплаєнс) ЛШ, гострота виникнення та розвитку АР (напр., при важкій гострій АР РНТ майже завжди короткий) та від аорто-шлуночкового градієнту тиску.
Ключові моменти: Щільність CW-спектру не дає цінної інформації щодо важкості АР. Визначення РНТ потребує коректного встановлення курсора CW. РНТ залежить від комплаєнсу та тисків в порожнинах, тому є лише додатковою ознакою важкості АР.
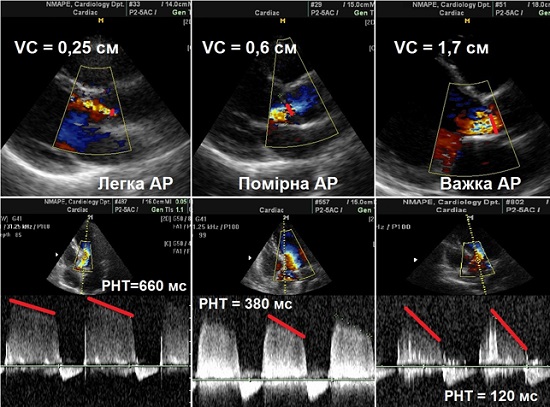
Рис. 10. Наведені три приклади КДК потоку АР в парастернальній позиції по довгій осі та відповідних CW-допплерівських спектрів АР в А5С позиції. По мірі збільшення ступеня АР ширина VC зростає, а РНТ прогресивно зменшується.
Вплив АР на розмір та функцію ЛШ
Важка АР призводить до важливих гемодинамічних ефектів, переважно на ЛШ. АР накладає додаткове об’ємне навантаження на ЛШ. При гострій АР ЛШ типово не є збільшеним, в той час як при хронічній АР ЛШ поступово та прогресивно дилатується з прогнозом незворотної дистрофії міокарду. Тому дилатація ЛШ є чутливою ознакою гемодинамічно значущої хронічної АР, а нормальні розміри ЛШ майже виключають важку хронічну АР. Втім, дилатація може спостерігатися при інших неспецифічних станах або бути відсутньою при гострій важкій АР.
Ключові моменти: в заключенні слід обов’язково відображати розміри, об’єми та ФВ ЛШ. Дуже рекомендується наводити індекси ромірів та об’ємів ЛШ до ППТ.
Інтегральна оцінка показників важкості
Ехокардіографічна оцінка АР включає поєднання даних 2D/3D візуалізації кореня Ао, АК та ЛШ, та допплерівських показників важкості регургітації (Таб. 4). Безсумнівно легкою є констатація легкої АР. В більш значущих випадках визначення ступіня АР може потребувати зусиль. Рекомендується використання максимально всіх методик, включаючи VC та PISA, де можливо. Допоміжні параметри допомагають дійти висновку щодо важкості АР та повинні широко застосовуватися при наявності розбіжностей між різними методиками, обов’язково зважаючи на клінічний контекст. Ці параметри слід інтерпретувати з урахуванням хронічності АР та ремоделювання ЛШ.
Таб. 4. Класифікація ступеней важкості АР.
|
Параметри
|
Легка
|
Помірна
|
Важка
|
|
Якісні
|
|
Морфологія АК
|
Нормальна / Ненормальна
|
Нормальна / Ненормальна
|
Ненормальна / Патологічна рухомість / Великий дефект коаптації
|
|
Ширина потоку АР в КДКа
|
Маленька при центральних потоках
|
Проміжна
|
Велика при центральних потоках / варіабельна при ексцентричнх
|
|
Спектр потоку АР в CW
|
Неповний / блідий
|
Щільний
|
Щільний
|
|
Реверсія діастолічного потоку в нисхідній Ао
|
Короткий протодіастолічний
|
Проміжний
|
Голодіастолічна (пікова швидкість >20 см/с)
|
|
Реверсія діастолічного потоку в брючній Ао
|
Відсутня
|
Відсутня
|
Наявна
|
|
Напівкількісні
|
|
Ширина VC (мм)
|
<3
|
3 – 6
|
≥6
|
|
Час напівзниження тиску РНТб
|
>500
|
200 – 500
|
<200
|
|
Кількісні
|
|
ПЕРО (cм2)
|
<0,10
|
0,10-0,19; 0,20-0,29г
|
≥0,30
|
|
ОР (мл)
|
<30
|
30-44; 45-59г
|
≥60
|
|
+ розміри ЛШв
|
|
|
|
а – При ліміті Найквіста 50–60 см/с.
б – РНТ скорочується при зростанні кінцево-діастолічного тиску в ЛШ, терапії вазодилататорами, у пацієнтів з податливою дилатованою Ао, або зростає при хронічній АР.
в – Якщо немає інших причин, розміри ЛШ звичайно нормальні у пацієнтів з легкою АР. При гострій важкій АР розміри ЛШ часто нормальні. Припустимі порогові значення для незначної дилатації ЛШ: КДР >5,6 см; іКДО >82 мл/м2; КСР >4,0 см; іКСО >30 мл/м2.
г – Помірна АР підрозділяється на легку помірну (ПЕРО = 0,10-0,19 см2 та ОР = 20-44 мл) та помірно важку (виражену) (ПЕРО = 0,20-0,29 см2 та ОР = 45-59 мл)
Легенева регургітація
Згідно даних літератури достатньо високий відсоток фізіологічної регургітації на нормальному клапані легеневої артерії (ЛР) зустрічається у здорових людей (40–78%). Набута легка та помірна ЛР часто спостерігається у пацієнтів з легеневою гіпертензією з чи без розширення легеневої артерії (ЛА). Важка ЛР зустрічається дуже рідко, звичайно у пацієнтів з анатомічними вадами клапану легеневої артерії (КЛА) чи після валвулотомії [19]. Існує дуже невелика кількість доказових досліджень внаслідок рідкісності випадків та труднощів візуалізації.
Анатомія та функція КЛА
КЛА – трьохстулкова структура, анатомічно подібна до АК (Рис. 11). Однак, структура КЛА є тоншою внаслідок нижчих значень тисків в правих відділах порівняно з лівими.
Етіологія та механізми
ЛР може бути викликана вродженими аномаліями (4-стулковий чи 2-стулковий клапани), гіпоплазією, станом після хірургічної корекції тетради Фалло або пролапсом КЛА. Інші причини включають інфекційний ендокардит, карциноїдний синдром. Карциноїдний синдром призводить до скорочення та потовщення стулок КЛА, подібно до залучення ТК. Міксоматозна дегенерація стулок КЛА є дуже рідкісним явищем, що призводить до потовщення та провисання стулок КЛА.
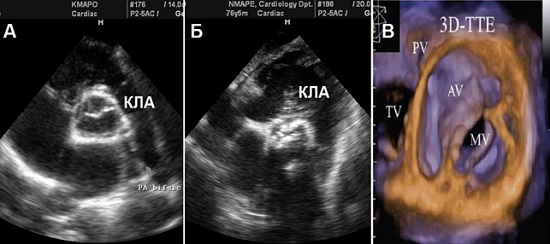
Рис. 11. Двохвимірні та 3D записи КЛА: А. Парастернальна позиція по короткій осі. Б. Субкостальна позиція. В. 3D-ЕхоКГ (PV – КЛА).
Ехокардіографічна оцінка ЛР
ТТЕхоКГ, ЧСЕхоКГ або 3D-ЕхоКГ можуть надати цінну інформацію відносно кількості стулок (2- чи 4-стулковий клапан), їх рухливості (натяжіння чи пролапс) та структури (гіпоплазія, дисплазія, відсутність КЛА). Втім, оцінка анатомії КЛА є складнішою порівняно з іншими клапанами внаслідок поганого акустичного доступу. Типово трансторакальної в В-режимі можливо візуалізувати тільки одну, максимум дві стулки КЛА одномоментно. Дуже рідко КЛА вдається візуалізувати по короткій осі. У дорослих візуалізація КЛА здійснюється з парастернальної позиції по короткій осі на рівні АК або з субкостального доступу. Роль ЧСЕхоКГ є обмеженною, тому що КЛА більш складно візуалізувати черезстравохідної (далеко від датчика). Зрізи, що дозволяють максимізувати візуалізацію КЛА включають горизонтальний зріз по короткій осні на рівні АК (зріз «притоку-відтоку») та глибокий шлунковий зріз з ротацією площини сканування на 120о (зріз виносного тракту).
Оцінка важкості ЛР
Оцінка важкості ЛР була менш обґрунтована, ніж АР.
Кольорова допплерографія
Кольорове допплерівське картування. Виявлення ЛР майже виключно базується на КДК. Діагностика ЛР – це документація діастолічного потоку в ВТПШ від КЛА. Патологічна ЛР відрізняється від фізіологічної довшою тривалістю (голодіастолічна) та ширшим потоком регургітації в місці виходу з КЛА [20]. Фізіологічна ЛР звичайно дуже маленька, центральна та витягнута. При важкій, коли вирівнювання діастолічного тиску в ЛА та в ПШ відбувається раніше в діастолі, кольорова площа потоку може бути скороченною та з не чіткими контурами (залежно від тисків) [21]. Оцінка важкості ЛР звичайно полягає в визначенні діаметру струменя регургітації в місці початку [22]. Максимальний діаметр кольорового струменя визначається в діастолу безпосередньо під КЛА (перехід ВТПШ в кільце КЛА) в парастернальній позиції по короткій осі чи з субкостального доступу. Хоча результати можуть бути дуже варіабельними залежно від оператора, звичайно ширина потоку більше 50-65% від діаметру ВТПШ говорить про важку ЛР [23]. Реєстрація реверсії діастолічного потоку в легеневих артеріях при КДК є дуже специфічною ознакою важкої ЛР.
Ширина VC. Хоча ширина VC мабуть є більш точним методом оцінки важкості ЛР, ніж ширина потоку, існує недостатньо доказових даних (Рис. 12 та 13). При цьому для ЛР діють ті самі обмеження, що і для інших клапанних регургітацій. У більшості випадків контур VC є складним. Цінність 3D-ЕхоКГ ще не була добре визначеною [24].
Метод конвергенції потоку. У деяких пацієнтів (дуже рідко при важкій ЛР) буває можливим оцінити зону конвергенції (Рис. 14). Втім, досліджень, які б оцінювали клінічну точність цієї методики для визначення важкості ЛР, не існує.
Імпульсний допплер
Теоретично PW-допплер антероградного та ретроградного потоків на рівні кільця КЛА та ЛА може бути використаний для розрахунку ОР та фракції регургітації. Діаметр кільця має вимірюватися підчас раннього вигнання (2–3 кадри після піку R на ЕКГ) безпосередньо під КЛА. Але ця методика несе багато можливостей похибки та не є добре валідованою [25].
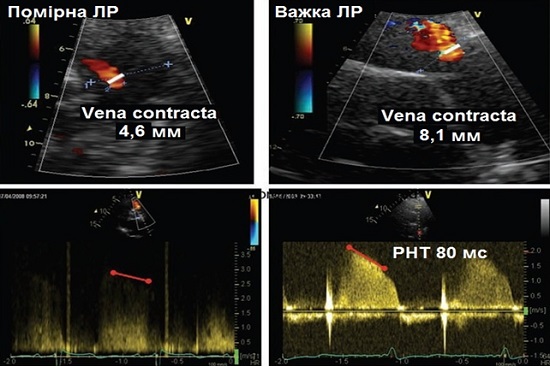
Рис. 12. Оцінка важкості ЛР за КДК. Зверху: виміри ВТПШ та ширини регургітуючого потоку; знизу – запис CW-спектрів ЛР
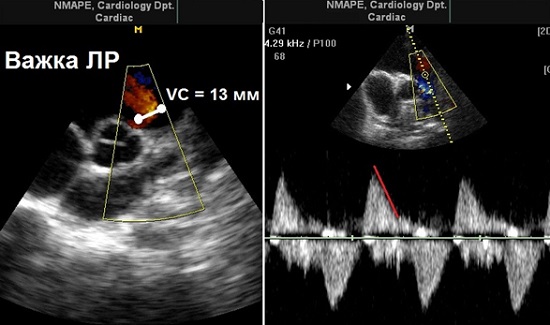
Рис. 13. Приклад пацієнта з важкою ЛР: зліва – відсутність коаптації стулок КЛА з виміром широкої VC; зправа – запис CW-спектрів ЛР з швидким сповільненням та раннім припиненням регургітуючого потоку перед кінцем діастоли та прискоренним систолічним кровотоком, не пов’язаним з супутнім стенозом КЛА.
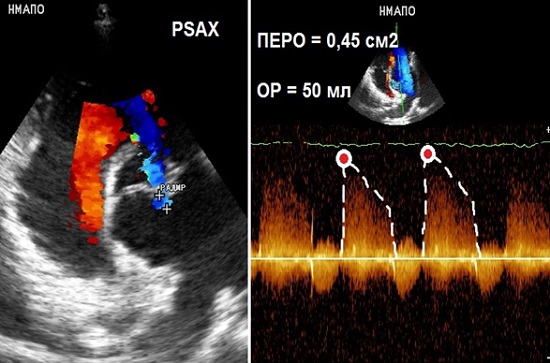
Рис. 14. Приклад визначення ПЕРО та ОР ЛР за методом PISA (доступний дуже в рідких випадках важкої ЛР.
Постійний допплер
Не існує клінічно одностайно прийнятого методу кількісної оцінки ЛР за даними CW-допплера. Щільність CW-сигналу надає певну якісну інформацію про важкість регургітації [26]. При легкій ЛР спостерігається повільне зниження швидкості регургітуючого потоку. Швидке сповільнення з припиненням потоку в середню чи пізню діастолу є неспецифічною ознакою важкої регургітації. У пацієнтів з вродженими вадами РНТ < 100 мс є чутливою та специфічною ознакою ЛР [27]. Час напівзниження тиску (РНТ) залежить не тільки від важкості ЛР, але й від діастолічного тиску в малому колі та діастолічних властивостей ПШ (скорочення РНТ при рестриктивній фізіології ПШ).
Наслідки ЛР
Оцінка розмірів та функції ПШ за відсутності легеневої гіпертензії забезпечує непрямі дані про важкість ЛР. Втім, наявність дилатації ПШ не є специфічною для важкої ЛР. Тим не менш, її відсутність говорить на користь більш легкого ступеня ЛР. Дилатація ПШ може спостерігатися при багатьох неспецифічних станах, а з іншого – бути відсутною при гострому виникненні ЛР. Функція ПШ класично оцінюється через визначення об’ємів ПШ та фракціонної зміни його площі (ФЗП ПШ). 3D-ЕхоКГ дозволяє більш точну оцінку ФВ ПШ. Клінічна цінність інших показників за даними тканинної допплерографії та спекл-трекінгу ще не має достатньо доказових засад, особливо в контексті ЛР, що не пов’язана з вродженими вадами серця.
Інтегральна оцінка показників важкості
Ехокардіографічна оцінка ЛР включає інтегральне сприйняття даних 2D/3D-візуалізації КЛА та ПШ з допплерівськими показниками важкості (Таб. 5). За відсутності достатньої кількості даних щодо кількісної оцінки ЛР експерти рекомендують оцінювати важкість ПШ, використовуючи всі можливі методики.
Ключові моменти: визначення важкості ЛР лишається складним внаслідок нечіткості існуючих стандартів. Вимір VC, мабуть, до сьогодні є найбільш точним підходом. Методика PISA може надати кількісну інформацію про важкість ЛР там, де її використання можливе. В усіх випадках рекомендується інтегральний підхід з урахуванням даних всіх використаних методик.
Таб. 4. Класифікація ступеней важкості ЛР.
|
Параметри
|
Легка
|
Помірна
|
Важка
|
|
Якісні
|
|
Морфологія КЛА
|
Нормальна
|
Нормальна / Ненормальна
|
Ненормальна
|
|
Ширина потоку ЛР в КДКа
|
Маленька, довжина звичайно <10 мм з вузьким витоком
|
Проміжна
|
Велика з широким витоком, може бути короткою за довжиною
|
|
Зворотний потік в легеневих артеріях
|
Відсутній
|
Відсутній
|
Наявний
|
|
Спектр потоку ЛР в CWб
|
Блідий
|
Щільний (варіабельно)
|
Щільний / швидке сповільнення, раннє припинення
|
|
Співвідношення легеневого до Ао потоку в PW
|
Нормальне або злегка підвищене
|
Проміжне
|
Значно підвищене
|
|
Напівкількісні
|
|
Ширина VC (мм)
|
Не визначена
|
Не визначена
|
Не визначена
|
|
Час напівзниження тиску РНТв
|
Не визначена
|
Не визначена
|
<100
|
|
Співвідношення ширини потоку
|
Не визначене
|
Не визначене
|
50-65%
|
|
Кількісні
|
|
ПЕРО (cм2)
|
Не визначена
|
Не визначена
|
Не визначена
|
|
ОР (мл)
|
Не визначений
|
Не визначений
|
Не визначений
|
|
+ розміри ПШг
|
|
|
|
а – При ліміті Найквіста 50–60 см/с.
б – Швидке сповільнення не є специфічною ознакою важкої ЛР.
в – РНТ скорочується при зростанні тиску в ПШ.
г – Якщо немає інших причин, розміри ПШ при легкій ЛР звичайно нормальні. При гострій важкій ЛР розміри ПШ часто нормальні. Прийняті порогові значення для легкого збільшення ПШ (розміри отримуються з А4С позиції): середній діаметр ПШ ≤33 мм, кінцево-діастолічна площа ПШ ≤28 см2, кінцево-систолічна площа ПШ ≤16 см2, ВЗП ПШ >32%.
Література
1. Zoghbi WA, Enriquez-Sarano M, Foster E, Grayburn PA, Kraft CD, Levine RA et al. Recommendations for evaluation of the severity of native valvular regurgitation with two-dimensional and Doppler echocardiography. J Am Soc Echo 2003;16:777–802.
2. Lancellotti P, Tribouilloy C, Hagendorff A, Moura L, Popescu BA, Agricola E et al. European Association of Echocardiography. European Association of Echocardiography recommendations for the assessment of valvular regurgitation. Part 1: aortic and pulmonary regurgitation (native valve disease). Eur J Echocardiogr 2010;11: 223–44.
3. Lancellotti P, Moura L, Pierard LA, Agricola E, Popescu BA, Tribouilloy Cet al. European Association of Echocardiography. European Association of Echocardiography recommendations for the assessment of valvular regurgitation. Part 2: mitral and tricuspid regurgitation (native valve disease). Eur J Echocardiogr 2010;11:307–32.
4. Lang RM, Badano LP, TsangW, Adams DH, Agricola E, Buck Tet al. EAE/ASE recommendations for image acquisition and display using three-dimensional echocardiography. Eur Heart J Cardiovasc Imaging 2012;13:1–46.
5. Carpentier A, Chauvaud S, Fabiani JN, Deloche A, Relland J, Lessana A et al. Reconstructive surgery of mitral valve incompetence: ten-year appraisal. J Thorac Cardiovasc Surg 1980;79:338–48.
6. Vahanian A, Alfieri O, Andreotti F, Antunes M, Baron-Esquivias G, Baumgartner H et al. Guidelines on the management of valvular heart disease (version 2012): the Joint Task Force on the Management of Valvular Heart Disease of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS). Eur Heart J 2012;33:2451–96.
7. Pierard LA, Lancellotti P. Stress testing in valve disease. Heart 2007;93:766–72.
8. Muraru D, Badano LP, Vannan M, Iliceto S. Assessment of aortic valve complex by three-dimensional echocardiography: a framework for its effective application in clinical practice. Eur Heart J Cardiovasc Imaging 2012;13:541–55.
9. deWaroux JB, PouleurAC, Goffinet C, et al. Functional anatomy of aortic regurgitation: accuracy, prediction of surgical repairability, and outcome implications of transesophageal echocardiography. Circulation 2007;116:I264–9.
10. Perry GJ, Helmcke F, Nanda NC, et al. Evaluation of aortic insufficiency by Doppler colour flow mapping. J Am Coll Cardiol 1987;9:952–9.
11. Tribouilloy CM, Enriquez-Sarano M, Bailey KR, et al. Assessment of severity of aortic regurgitation using the width of the vena contracta: a clinical color Doppler imaging study. Circulation 2000;102:558–64.
12. Eren M, Eksik A, Gorgulu S, Norgaz T, , et al. Determination of vena contracta and its value in evaluating severity of aortic regurgitation. J Heart Valve Dis 2002;11:567–75.
13. Fang L, Hsiung MC, Miller AP, et al. Assessment of aortic regurgitation by live three-dimensional transthoracic echocardiographic measurements of vena contracta area: usefulness and validation. Echocardiography 2005; 22:775–81.
14. Tribouilloy CM, Enriquez-Sarano M, Fett SL, et al. Application of the proximal flow convergence method to calculate the effective regurgitant orifice area in aortic regurgitation. J Am Coll Cardiol 1998;32:1032–9.
15. Pouleur AC, deWaroux JB, Goffinet C, et al. Accuracy of the flow convergence method for quantification of aortic regurgitation in patients with central versus eccentric jets. Am J Cardiol 2008;102:475–80.
16. Tribouilloy C, Avine´e P, Shen WF, et al.. End diastolic flow velocity just beneath the aortic isthmus assessed by pulsed Doppler echocardiography: a new predictor of the aortic regurgitant fraction. Br Heart J 1991;65:37–40.
17. Samstad SO, Hegrenaes L, Skjaerpe T, et al. Half time of the diastolic aortoventricular pressure difference by continuous wave Doppler ultrasound: a measure of the severity of AR?. Br Heart J 1989;61:336–43.
18. Griffin BP, Flachskampf FA, Siu S, et al. The effects of regurgitant orifice size, chamber compliance, and systemic vascular resistance on aortic regurgitant velocity slope and pressure half-time. Am Heart J 1991;122:1049–56.
19. Bouzas B, Kilner PJ, Gatzoulis MA. Pulmonary regurgitation: not a benign lesion. Eur Heart J 2005;26:433–9.
20. Maciel BC, Simpson IA, Valdes-Cruz LM, et al. Color flowDopplermapping studies of ‘physiologic’ pulmonary and tricuspid regurgitation: evidence for true regurgitation as opposed to a valve closing volume. J Am Soc Echocardiogr 1991;4:589–97.
21. Kobayashi J, Nakano S, Matsuda H, , et al. Quantitative evaluation of pulmonary regurgitation after repair of tetralogy of Fallot using real-time flow imaging system. Jpn Circ J 1989;53:721–7.
22. Williams RV, Minich LL, Shaddy RE, , et al. Comparison of Doppler echocardiography with angiography for determining the severity of pulmonary regurgitation. Am J Cardiol 2002;89:1438–41.
23. Puchalski MD, Askovich B, Sower CT, , et al. Pulmonary regurgitation: determining severity by echocardiography and magnetic resonance imaging. Congenit Heart Dis 2008;3:168–75.
24. Pothineni KR,Wells BJ, Hsiung MC, et al. Live/real time three-dimensional transthoracic echocardiographic assessment of pulmonary regurgitation. Echocardiography 2008;25:911–7.
25. Goldberg SJ, Allen HD. Quantitative assessment by Doppler echocardiography of pulmonary or aortic regurgitation. Am J Cardiol 1985;56:131–5.
26. Lei MH, Chen JJ, Ko YL, et al. Reappraisal of quantitative evaluation of pulmonary regurgitation and estimation of pulmonary artery pressure by continuous wave Doppler echocardiography. Cardiology 1995;86:249–56.
27. Silversides CK, Veldtman GR, Crossin J, et al. Pressure Halftime predicts hemodynamically significant pulmonary regurgitation in adult patients with repaired tetralogy of Fallot. J Am Soc Echocardiogr 2003; 16:1057–62.