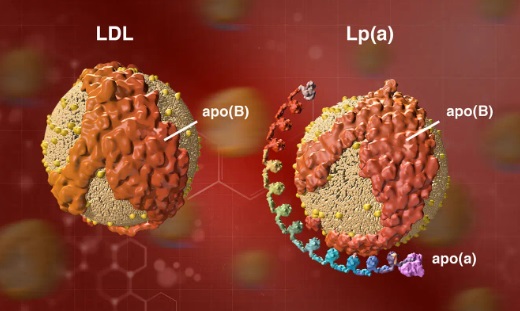
 Результати нового дослідження показали значний зв’язок між рівнями Lp(a) та коронарним атеросклерозом із ознаками високого ризику.
Результати нового дослідження показали значний зв’язок між рівнями Lp(a) та коронарним атеросклерозом із ознаками високого ризику.
Вплив Lp(a) на ендотелій коронарної артерії посилює прогресування бляшок на коронарних артеріях і перикоронарне запалення, а також сприяє розвитку бляшок низької щільності.
Пацієнти з рівнями Lp(a) ≥125 нмоль/л мали вдвічі більший відсоток об’єму атероми (6,9% проти 3,0%; p = 0,01), і після коригування інших факторів ризику кожне подвоєння Lp(a) призводило до додаткового збільшення відсотка об’єму атероми на 0,32% протягом 10 років спостереження.
У цьому одноцентровому проспективному когортному дослідженні брали участь 299 пацієнтів з підозрою на ішемічну хворобу серця (ІХС), які пройшли комп'ютерну томографічну коронарографію (КТК) з інтервалом між скануваннями 10 років. Тридцять два пацієнти були виключені через аортокоронарне шунтування, в результаті чого досліджувана популяція складалася з 267 пацієнтів. Середній інтервал сканування становив 10,2 року. Lp(a) вимірювали під час подальшого спостереження за допомогою ізоформ-інсенситивного аналізу. Взаємозв’язок між Lp(a) і зміною процентного об’єму бляшок був досліджений у лінійних моделях змішаних ефектів з урахуванням клінічних факторів ризику. Вторинними результатами були наявність бляшок низької щільності та наявність підвищеного згасання перикоронарної жирової тканини на початковому рівні та при подальшій візуалізації за допомогою КТК.
Середній вік досліджуваної популяції становив 57,1 (стандартне відхилення, 7,3) років і 153 були чоловіками (57%). Пацієнти з рівнями Lp(a) ≥125 нмоль/л мали вдвічі більший відсоток об’єму атероми (6,9% проти 3,0%; p = 0,01) порівняно з пацієнтами з рівнями Lp(a) <125 нмоль/л. З поправкою на інші фактори ризику кожне подвоєння Lp(a) призводило до додаткового збільшення на 0,32% (95% довірчий інтервал [ДІ], 0,04-0,60) відсотка об’єму атероми протягом 10 років спостереження. Кожне подвоєння Lp(a) призводило до співвідношення шансів 1,23 (95% ДІ, 1,00-1,51) і 1,21 (95% ДІ, 1,01-1,45) для наявності бляшок низької щільності на початковому етапі та в період спостереження відповідно. Пацієнти з вищим рівнем Lp(a) мали підвищене згасання перикоронарної жирової тканини навколо правої коронарної артерії та лівої передньої низхідної артерії на початковому рівні та в період спостереження.
Науковці зазначають, що у цьому довгостроковому проспективному дослідженні серійної візуалізації КТК вищі рівні Lp(a) були пов’язані зі збільшенням прогресування навантаження коронарних бляшок і збільшенням наявності некальцифікованих бляшок низької щільності та запалення перикоронарної жирової тканини. Ці дані свідчать про довгостроковий вплив підвищених рівнів Lp(a) на коронарний атерогенез запальних бляшок високого ризику, схильних до розриву.
Результати показали значний зв’язок між рівнями Lp(a) та коронарним атеросклерозом із ознаками високого ризику. Дослідження, що оцінюють терапію, яка знижує Lp(a) і клінічні результати, тривають і можуть виявити інший варіант лікування для пацієнтів з високим ризиком атеросклерозу.
Літературні посилання знаходяться в редакції Webcardio.org